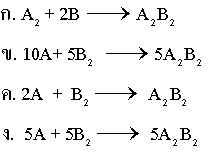|
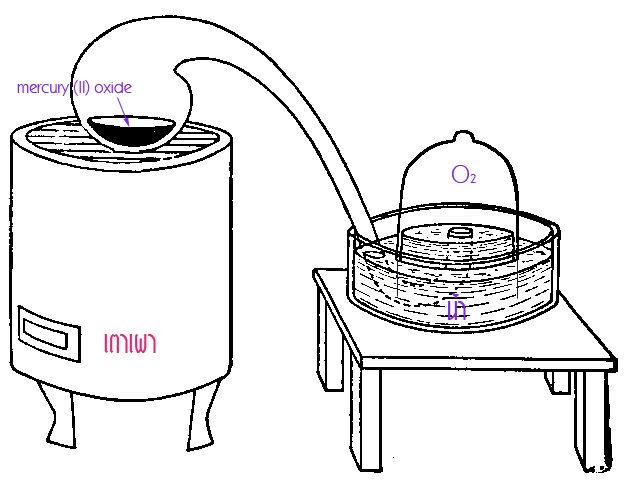
ลาวัวซิเยร์ : กฎทรงมวล เมื่อเคมีสมัยใหม่เริ่มต้นในศริสตศตวรรษที่ 18 นักวิทยาศาสตร์เริ่มที่จะสังเกตปริมาณของสาร จากการทดลองของลาวัวซิเยร์ เพื่อแยกแก๊สออกซิเจนออกมา ในการทดลองของ ลาวัวซิเยร์ มีอุปกรณ์ที่เกี่ยวข้องดังรูป ด้านล่าง โดยที่นำเมอร์คิวรี่(II)ออกไซด์ใส่ลงไปในขวดคอยาวโดยที่คอขวดต่ออยู่กับครอบแก้วรูประฆังมีปริมาตร 40 ลูกบาศก์นิ้วสำหรับเก็บแก๊สที่เผาได้ โดยใช้เตาเผาที่มีถ่าน (charcoal) เป็นเชื้อเพลิง เขาได้ชั่งน้ำหนักของสารเริ่มต้น ก่อนเผาไว้ จากนั้นทำการเผา เมอร์คิวรี่(II)ออกไซด์ เป็นเวลา 12 วัน จะสังเกตได้ว่าระดับน้ำในขวดรูประฆังลดลงแสดงว่าต้องมีแก๊สเกิดขึ้น ทดสอบโดยการจุดเทียนไขได้เปลวไฟที่สว่าง มากกว่าปกติ ส่วนในขวดคอยาวพบว่ามีปรอทเหลว(mercury)
จากการชั่งน้ำหนักของสารตั้งต้นในขวดคอยาว และผลิตภัณฑ์ เขาพบว่ามวลโดยรวมของผลิตภัณฑ์ มีมวลเท่ากับเมอร์คิวรี่(II)ออกไซด์ที่เริ่มต้น เขาจึงสรุปออกมาเป็นกฎทรงมวล ว่า "มวลของสารก่อนทำปฏิกิริยาจะเท่ากับมวลของสารหลังทำปฏิกิริยา" ดังนั้น การเผาเมอร์คิวรี่(II)ออกไซด์ (เมอร์คิวริก ออกไซด์)จะให้ผลิตภัณฑ์ออกมา 2 ชนิด ได้แก่ เมอร์คิวรี่ (ปรอทเหลว) และแก๊สออกซิเจน ดังสมการ
ตัวอย่างที่ 1 แวน เฮลมองต์(Van Helmont) ได้ทดลองปลูกต้นหลิวไว้ในกระถางซึ่งใช้ดินปลูก หลังจาก 5 ปีผ่านไปเขาพบว่าน้ำหนักของต้นหลิวเพิ่มขึ้น 75 กิโลกรัม แต่ดินมีมวลลดลงเพียง 0.057 กิโลกรัม เขาเติมน้ำเพียงอย่างเดียวลงในกระถาง เขาจึงสรุปได้ว่ามวลที่เพิ่มขึ้นมาจากน้ำ จงอธิบายและวิเคราะห์เหตุผล แนวคิด การอธิบายของ แวน เฮลมองต์ ในกฎทรงมวล ยังมีส่วนที่ขาดหายไปเนื่องจาก มวลที่เพิ่มขึ้นของต้นไม้ต้องขึ้นอยู่กับปฏิกิริยาของคาร์บอนไดออกไซด์ในการเจริญเติบโตอีกด้วย หรืออาจจะกล่าวได้ว่า ต้นไม้เติบโตได้โดยใช้คาร์บอนไดออกไซด์ในอากาศ แร่ธาตุต่างๆ จากดิน และน้ำ
Joseph Proust
เป็นผู้ก่อตั้งกฎนี้ขึ้นมา เขากล่าวว่า สารที่เป็นสารประกอบชนิดเดียวกันมีองค์ประกอบที่เหมือนกัน
เช่น
ตัวอย่างที่ 2 ในการเกิดโมเลกุลของน้ำจะต้องใช้ ไฮโดรเจน 2 โมล รวมกับ ออกซิเจน 1 โมล จึงได้โมเลกุลของน้ำ 2 โมล ซึ่งจะเป็นอัตราส่วนอย่างนี้ตลอดไป แสดงได้ดังรูปภาพด้านล่าง
ตัวอย่างที่ 3 ปฏิกิริยาระหว่าง A (อะตอม สีฟ้า)กับ B(อะตอม สีเงิน) ดังรูป
สมการเคมีข้อใดที่อธิบายปฏิกิริยานี้ตามกฎทรงมวล
แนวคิด ตามกฎทรงมวลจำนวนอะตอมทั้ง 2 ข้างของสมการต้องเท่ากัน จากรูป ด้านซ้ายมือ นับอะตอมสีฟ้าซึ่งเป็นโมเลกุลอะตอมเดี่ยว ก็คือ A นับได้ทั้งหมด 10 โมเลกุล ส่วนโมเลกุลสีน้ำเงินเป็นโมเลกุลอะตอมคู่ก็คือ B2 นับได้ทั้งหมด 5 โมเลกุล จากรูปทางขวามือ เมื่อทำปฏิกิริยาแล้วจะได้โมเลกุลที่ประกอบด้วย A2B2 นับได้ทั้งหมด 5 โมเลกุล ดังนั้น สามารถเขียนแทนด้วยสมการเคมี คือ
ทำให้เป็นอัตราส่วนอย่างต่ำ โดย หารด้วย 5 ทั้งสมการ จะได้สมการคือ
|